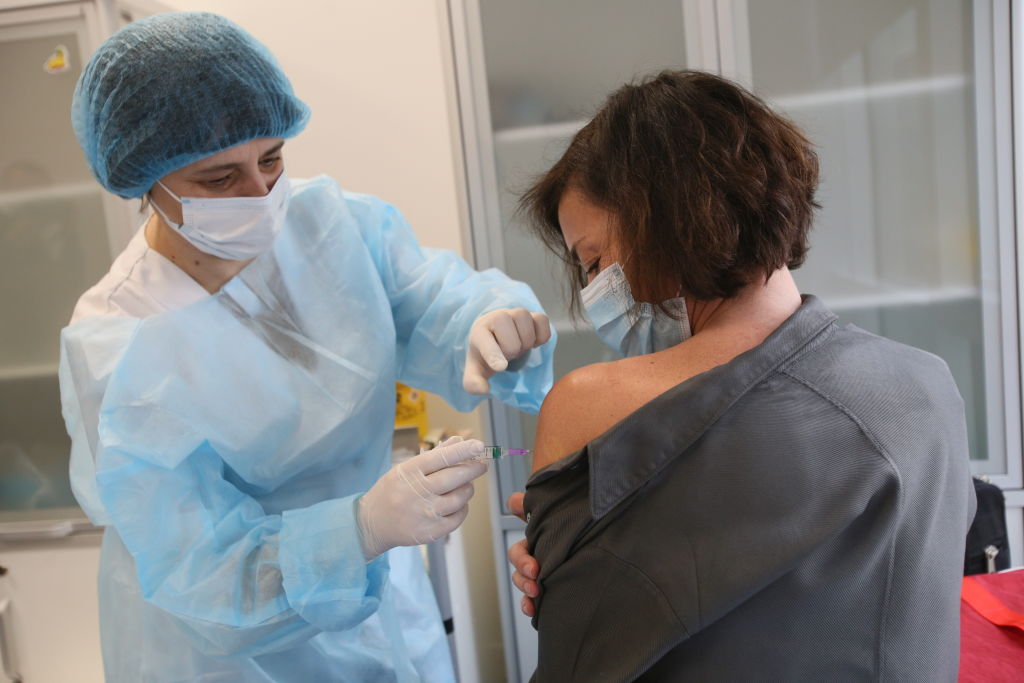
С начала вакцинальной кампании в Украине в социальных сетях идут бурные дискуссии о безопасности вакцин от ковида. Иногда в таких спорах используются совершенно очевидные и даже забавные в своей очевидности фейки-страшилки вроде того, что РНК-вакцина “встраивается в генетический код человека” или что “вакцина медленно убивает и все вакцинированные умрут через два года”. Но многие люди высказывают вполне понятные сомнения насчет того, насколько хорошо изучено действие вакцины. Ведь создали ее так быстро — с начала объявленной ВОЗ пандемии коронавируса прошло всего лишь 9 месяцев, когда компания Prizer объявила об окончании клинических испытаний вакцины Prfizer/BionTech.
Действительно ли процесс создания вакцины от коронавируса SARS-CoV-2 так уж сильно отличался от того, как создавались и испытывались давно всем известные вакцины от кори, полиомиелита, ветрянки? И каким образом удалось разработать вакцину такими темпами, соблюдая все требования к ее безопасности?
На этот вопрос отвечает врач Ольга Шварацкая, кандидат медицинских наук, доцент кафедры педиатрии 3 и неонатологии Днепропетровского медицинского университета, член Европейского общества детских инфекционных болезней (ESPID), Европейской академии аллергии и клинической иммунологии (EAACI) и Европейского респираторного общества (ERS).

Ни сам вирус, ни технология создания вакцин не были такими уж “новыми”
Во-первых, некоторые важные особенности иммунного ответа на коронавирусы были выяснены еще до появления SARS-CoV-2. В начале двухтысячных был первый SARS-CoV («атипичная пневмония») в Китае, а в 2012 появился МЕRS-CoV (ближневосточный тяжелый респираторный синдром) в Саудовской Аравии – два суровых коронавируса. У этих вирусов — предшественников нынешнего коронавируса были похожие ключевые белки (S-протеин, или спайк-белок), которые выступают мишенью для нашей иммунной системы, если она встретится с вирусом.
Вакцины против SARS-CoV и МЕRS-CoV, нацеленные на такой спайк-белок, уже находились в процессе испытаний на животных, а некоторые – даже в первой фазе клинических исследований с участием людей. Это сэкономило много времени, которое могло бы быть потрачено на выбор подходящей «мишени» для иммунитета, если бы вирус оказался абсолютно новым и не похожим ни на что ранее изученное.
Во-вторых, те типы вакцин, которые мы называем «новыми», а именно векторные вакцины (как AstraZeneka или Johnson&Johnson) и вакцины на основе нуклеиновых кислот (как Pfizer или Moderna) – не такие уже и новые. Технологии, лежащие в основе этих вакцин, придумали еще два-три десятилетия назад.
В 2019 году уже были исследованы и зарегистрированы несколько векторных вакцин от лихорадки Эбола, клинических испытания проходили векторные вакцины против ВИЧ, гриппа, вируса Зика и того же МЕRS-CoV.
Также в клинических исследованиях уже несколько лет находились ДНК-вакцины против лихорадки Эбола и Зика, гриппа, МЕRS; а еще РНК-вакцины против ВИЧ, гриппа, бешенства, лихорадки чикунгунья.
Правда, до регистрации ни одна из них на тот момент не дошла. Но у животных такие вакцины уже применялись (например, ДНК-вакцина против лихорадки Западного Нила у лошадей).
Более того, векторные и ДНК/РНК технологии уже считались подходящими кандидатами для экстренной разработки нужных вакцин в случае появления нового злобного патогена, потому что их достаточно быстро можно адаптировать под разных возбудителей.
В-третьих, РНК нового коронавируса расшифровали очень быстро, она была опубликована в научном журнале уже 10 января 2020 года — когда большинство из нас еще вообще были не в курсе всей этой истории, и уж точно предположить не могли, во что она выльется.
Что еще важно, новый возбудитель оказался достаточно стабилен в сравнении со своими собратьями – другими РНК-вирусами, такими как грипп или ВИЧ. Он не очень быстро меняет свои важные для иммунитета места, хотя из новостных потоков о «новых штаммах» может показаться иначе. Поэтому вакцины, созданные под структуру исходного варианта вируса, в той или иной мере эффективны против разнообразных новых вариантов.
Как только РНК была расшифрована, разработчики немедленно приступили к созданию вакцины и фактически завершили основные работы в январе-феврале 2020 года. А быстрому клиническому исследованию и выходу на рынок способствовала невиданная ранее вовлеченность научного сообщества и небывалое финансирование.

Фото: Getty Images
На фото: премьер-министр Австралии Скотт Моррисон посещает производство вакцин в феврале 2020 года.
Как выглядит классический процесс разработки вакцин?
Процесс исследования и признания лекарственных препаратов и вакцин в мире строго определен и достаточно унифицирован. Он включает много правил, которые нужно соблюдать, чтобы получить международное признание. А количество степеней защиты от попадания на рынок лекарственных препаратов и вакцин какой-то новой бесполезной или, не дай бог, вредоносной ерунды в Европе и Америке достаточно велико.
Вакцину создают (этот процесс в англоязычном мире называется “дизайном вакцины”), производят несколько десятков или сотен доз и начинают испытывать на животных. На данном этапе в первый раз оценивают безопасность вакцины и ее иммуногенность (то есть способность вызывать иммунный ответ после прививки). Обычно этот этап длится от нескольких месяцев до года. Параллельно отлаживают процесс производства вакцины в больших масштабах, готовясь к массовым клиническим исследованиям, то есть исследованиям с участием людей.
Затем начинаются собственно клинические исследования. На этом этапе снова изучается безопасность вакцины, ее иммуногенность, уточняются дозировки, а еще проверяется эффективность.
В первой фазе клинических испытаний всегда участвует лишь несколько десятков здоровых взрослых людей, во второй – несколько сотен, а в третьей — уже тысячи или десятки тысяч добровольцев, причем не только молодых и полностью здоровых, но и других возрастов, с хроническими заболеваниями и пр. То есть разнообразие участников существенно ближе к реальной жизни.
Начинается третья фаза тогда, когда на основании результатов предыдущих двух этапов становится понятно, что новая вакцина никаких частых и серьезных проблем в организме не вызывает и дает хороший иммунный ответ (производство антител). По результатам третьей фазы судят об эффективности вакцины — то есть о том, насколько реже вакцинированные заражаются данной инфекцией, насколько реже они болеют тяжело и умирают, насколько реже заражают других.
В течение всех трех фаз следят за побочными эффектами вакцины, и, естественно, чем больше людей участвуют в испытаниях, тем больше редких побочных эффектов можно выявить.
Фаза 3 обычно длится от полутора до пяти лет. После ее окончания и публикации результатов в авторитетных научных изданиях производитель подает документы в регуляторные органы для лицензирования. А также окончательно отлаживает и сертифицирует широкомасштабное производство для выхода на рынок.
Рассмотрение документов до лицензирования раньше могло длиться один-два года, никто никуда не торопился. Таким образом, весь процесс от появления идеи до выхода на рынок занимал 5-10 лет.
Затем наступает фаза 4 — уже не испытания, а наблюдения за тем, как вакцина применяется и действует в реальном мире, а не в контролируемых группах. Это не эксперимент и не «опыты»! Это обсервационные исследования, исследователь просто мониторит и собирает данные, не регулируя процесс и не вмешиваясь.
Чтобы регистрировать побочные эффекты вакцин, в мире создана международная система VAERS (Vaccine Adverse Events Reporting System), а у отдельных стран есть национальные системы мониторинга. В Украине это Автоматизированная информационная система по фармаконадзору (АІСФ), куда могут подавать информацию о побочных эффектах не только медицинские работники, но и пациенты.
То есть никто ничего не скрывает, — наоборот, стараются создать условия, чтобы узнать как можно больше, в том числе напрямую от пациентов.
И это нормальная практика – выпустить препарат на рынок, а потом уже отлавливать редкие поствакцинальные события. Потому что в случае с редкими и очень редкими побочными эффектами польза от применения вакцины почти всегда превышает риск.
Вспомним, например, сообщения о тромбах, которые обнаруживались после вакцинации векторными вакцинами. Их частота которых даже по самым суровым оценкам в общей популяции не превышает 1:100 000. Их не видно было в третьей фазе не потому, что «плохо исследовали из-за спешки». А потому, что сотни тысяч людей в третью фазу и раньше, в доковидную эпоху, не принято было набирать.
Этот очень редкий побочный эффект все равно бы зарегистрировали уже после выхода на рынок, даже если исследования велись бы по классической схеме, как раньше. То же касается повышенной частоты анафилаксии после мРНК-вакцин.
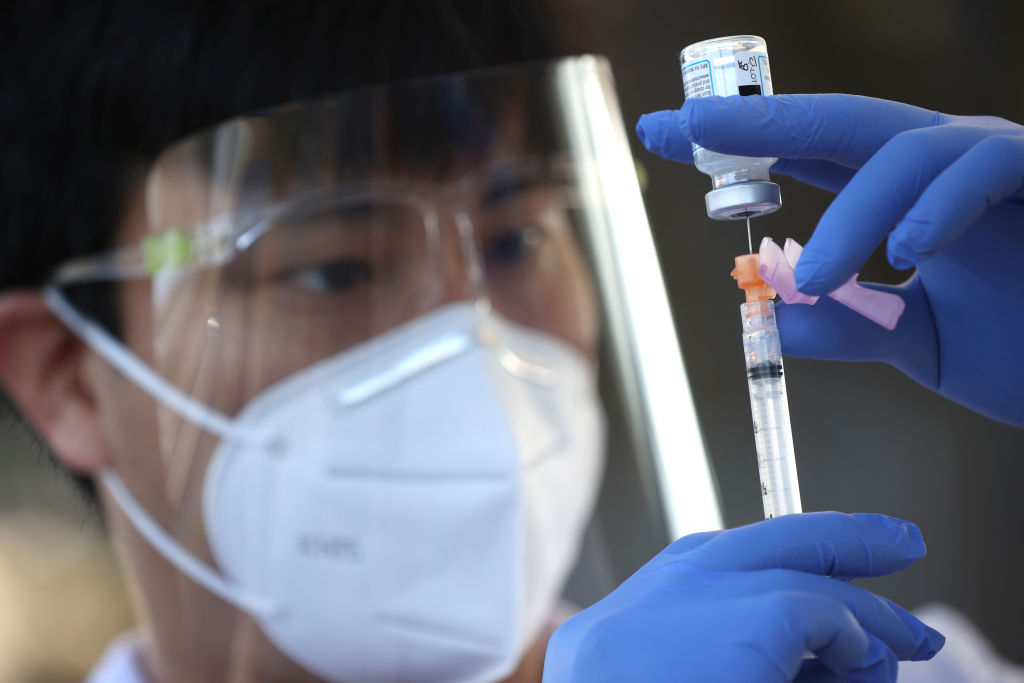
Фото: Justin Sullivan/Getty Images
Как ускорили исследования вакцин от ковида?
Процесс проведения исследований вакцин был изобретательно адаптирован к требованиям срочности. При этом, понятно, жертвовать качеством и безопасностью было нельзя.
Все этапы и фазы исследований вакцины были точно такими же, как и в допандемические времена. Количество участников в фазах – тоже. Этого никто не менял, на структуре и количестве не экономили.
Вопреки расхожим мемам, вакцина в самом начале была испытана на животных — в основном на обезьянах и хорьках, так как они заражаются и болеют коронавирусом.
Однако по международному соглашению этапы и фазы исследований начали проводить «внахлест». То есть решение о начале следующего этапа принималось на основании не окончательных, а предварительных результатов предыдущего. Фаза 1 клинических исследований началась еще до завершения исследований на животных, фаза 2 – с середины первой фазы и так далее. При этом саму длительность каждого этапа старались сильно не сокращать.
Волонтеров набирали очень быстро и активно, благо, желающих хватало.
Производители очень рано начали окончательное масштабирование производства – еще на уровне фазы 1, а не фазы 3, как раньше. Для них это был огромный финансовый риск, потому что если бы что-то пошло не так, исследования были бы остановлены и эти огромные вложения никогда бы не возместились.
Так, кстати, и произошло с несколькими вакцинами-кандидатами, о которых широко не известно, потому что они остановились достаточно рано.
Ну и наконец, ряд регуляторных органов сменил подход для ускорения процесса. Раньше весь пакет документов для лицензирования принимался одномоментно после фазы 3. В случае вакцин от ковида, европейский регулятор (ЕМА), например, принимал промежуточные отчеты от исследовательских центров и производил оценку данных каждые две недели. Это существенно ускорило процесс лицензирования.
И поскольку основная задача третьей фазы – это все-таки уточнение эффективности, а не вопросы безопасности (уже решенные фазами 1-2), то вакцины были условно одобрены европейскими и американскими регуляторами на основании предварительных, а не окончательных результатов третьей фазы.
Почему раньше так не делали? До 2020 года для этого не было юридических норм и разрешений; у производителей не было мотивации рисковать финансами, а у добровольцев – организмом.
Где мы сейчас? Фазы 3 уже зарегистрированных вакцин еще продолжаются и продлятся еще пару лет. В них собирают дополнительные данные об эффективности вакцин у тех категорий людей, которые не были включены в начале, – детей, беременных женщин.
Продолжаются наблюдения за применением и эффективностью вакцины «в реальной жизни» ‒ абсолютно так же, как раньше.
Появляются новые вакцины-кандидаты и продвигаются по пути исследований старые, но еще не одобренные. 93 вакцины-кандидата сейчас находятся в стадии клинических исследований, и еще минимум 77 – в доклинической стадии.
Через несколько лет мы окончательно узнаем, какие вакцины оказались самыми эффективными, как они работают с новыми вариантами вируса, как долго держится иммунная защита после вакцинации.

Фото: AFP via Getty Images
А что если “побочка” начнется только через год или пять лет после прививки?
Вся серьезная негативная побочка после вакцинации, если уж случается, то в абсолютном большинстве случаев ‒ в течение первых месяца-двух после вакцинации. Или к этому времени уже видны предпосылки, по которым можно предположить потенциальные долгосрочные последствия.
Поэтому одним из критериев американского FDA для одобрения вакцин против COVID-19 было наличие данных по безопасности вакцины в течение двух месяцев после вакцинации. Они не с потолка эту цифру взяли.
Надо заметить, что наблюдать за участниками исследования по 10 лет еще до регистрации вакцины никто и раньше не думал. Это было не принято, вопреки расхожему мнению.
Для тех, кто продолжает беспокоиться о гипотетических «долгосрочных» последствиях, приятный бонус: не всегда то, что выясняется о вакцинах спустя время, – плохо. Например, оказалось, что дети, вакцинированные в младенчестве от ротавируса, через 5-10 лет существенно реже заболевают сахарным диабетом первого типа.
Первоисточник на странице Ольги Шварацкой в Facebook цитируется с согласия автора.
Читайте также:
Надо ли вакцинироваться от коронавируса, если вы уже переболели? Поясняет врач
Венгрия первой из стран ЕС признала украинское свидетельство о вакцинации от COVID-19
После вакцинации заболеваемость COVID-19 резко снизилась — исследование